سازمان غذا و داروی آمریکا (FDA) روز ۱۴سپتامبر ۲۰۱۷ برای داروی جدیدی بهنام(Aliqopa (Copanlisib مجوز «تأییدیه تسریعشده (Accerelated Approval Regulation)» داد. این دارو برای درمان لنفومفولیکولار عود کرده (Elapsed F. L) در بزرگسالانی که درگذشته حداقل ۲بار درمانهای پیشین سیستمیک را دریافتکردهاند بهکاربرده میشود.
دکتر ریچاردپازدور(Dr.Pazdur) مدیر مرکز آنکولوژی و هماتولوژی FDA بیانمیدارد: «در بیماران با لنفومفولیکولار عودکرده، حتی پساز چند دورهدرمان، بیماری اغلب برگشت میکند و این درحالی است که گزینههای درمان برای این بیماران محدود بوده و تأیید یک درمان جدید، یک انتخاب بیشتر را برای آنان فراهم کرده و یک کمبود را برای آنان جبران مینماید».
لنفوم فولیکولار یک بدخیمی سیستم لنفاوی با رشد آهسته از نوع لنفوم غیرهوچکینی است. سیستم لنفاوی بخشیاز سیستمایمنی بدن بوده و از بافتهایلنفاوی، عقدههایلنفاوی، طحال، تیموس، لوزهها و مغزاستخوان تشکیل شدهاست. مؤسسه ملی سرطان آمریکا(NCI) تخمینمیزند که درسال جاری تنها در آمریکا حدود ۷۲۲۴۰ تَن مبتلا به برخیاز انواع لنفومای غیرهوچکینی میشوند و حدود ۲۰۱۴۰بیمار با لنفوم غیرهوچکینی بهدلیل ابتلا به این بیماری تا پایان سال۲۰۱۷ فوتمینمایند.
Aliqopa یک مهارکننده کیناز است که ازطریق مهار چند آنزیم که محرک رشد سلولی هستند، عملمیکند.
قانون«تأییدیه تسریعشده» که در بالا به آن اشارهگردید (Accerelated Approval Regulation)»، FDA را قادرمیسازد تا داروهاییکه برای برآوردن یک نیاز پزشکی حتمی در بیماریهای جدی مورد نیاز است را تأییدنماید. این تأیید ازطریق استفادهاز اطلاعات کارآزمایی بالینی صورتمیگیرد و بهنظرمیرسد برای بیماران استفاده بالینی دارد.آزمایشات بالینی بیشتری برای تأیید فایده بالینی Aliqopa موردنیاز است و حامی مالی این دارو، درحالحاضر این تحقیقات را هدایت میکند.
تأیید این دارو براساس اطلاعاتی از یک کارآزمایی تکبازویی (Single-Arm Trial) شامل ۱۰۴ بیمار با لنفوم B Cell غیرهوچکینی انجامشد که حداقل ۲دوره درمان عود داشتهاند. دراین آزمایش بیمارانیکه جمعشدگی کامل یا بخشیاز تومور را بعداز درمان داشتند، مورد بررسی قرارگرفتند؛ ۵۹ درصد از این بیماران بهصورت کامل یا جزئی بعداز مدت متوسط ۱۲/۲ماه به درمان پاسخ دادند.
عوارض جدی شایع این دارو شامل افزایش قندخون، اسهال، کاهش قدرت و انرژی عمومی، فشارخون بالا، کاهش گلبولهای سفید (لکوپنی،نوتروپنی)، تهوع و عفونتهای مجاری تنفسی تحتانی و کاهش سطح پلاکت های خون (ترومبوسیتوپنی) میباشد.
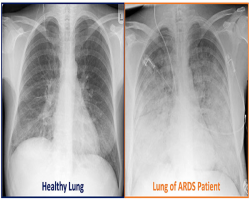
عوارضجانبی جدی شامل عفونتها، قند خون بالا، فشارخون بالا، التهاب بافت ریه (پنومونیت غیرعفونی)، افت گلبولهایسفید خون(نوتروپنی) و واکنشهای پوستی شدید میباشد.
در زنان باردار و یا در مرحله شیردهی بهدلیل آنکه این دارو میتواند به تکامل جنین یا نوزاد تازه متولدشده آسیب واردنماید، بهتراست از Aliqopa استفاده نشود.
Aliqopa درگروه «بازنگری در اولویت» (Piority Review) قرارداده شدهاست. هدف FDA ازاین دستهبندی، بررسی عملکرد یک دارو درطی ۶ماه پس از تأیید آن دارو میباشد تا مشخص شود که دارو دراینمدت بهطورمشخص سلامت (Safe) بوده و یا اثربخشی واضحی در درمان و یا در تشخیص و یا پیشگیری یک بیماری جدی نقش مهمی داشته است یا خیر.
Aliqopa همچنین درگروه داروهای Orphan Drug Act قرارداده شدهاست که به گروهیاز داروها که انگیزه برای کمک و تشویق تکامل داروهایی را برای درمان بیماریهای نادر فراهممینمایند، اطلاقمیشود.
FDA امتیاز داروی Aliqopa را بــه شرکت Bayer Healthcare Pharmaceuticals بخشیده است.










ثبت نظر