99-133
اندوتلیال عروقی ریوی، ترومبوز و آنژیوژنز در بیماری کووید-19
منبع :شمارۀ 1235 نشریه پزشکی امروز
نارساییپیشرفتۀتنفسی(Progressive respiratory failure) ، بهعنوان اصلیترین عامل مرگومیر در همهگیری اخیر ناشی از کووید-19 نقش اساسی داشته است.پاتوفیزیولوژی این بیماری بصورت گسترده شناخته شده است، اما به لحاظ تغییرات مورفولوژی (ریختشناسی) و مولکولی در ریههای محیطی بیمارانی که به دلیل ابتلا به این بیماری جان خود را از دست دادهاند ، نسبتا ناشناخته ماندهاست.
نارساییپیشرفتۀتنفسی(Progressive respiratory failure) ، بهعنوان اصلیترین عامل مرگومیر در همهگیری اخیر ناشی از کووید-19 نقش اساسی داشته است.پاتوفیزیولوژی این بیماری بصورت گسترده شناخته شده است، اما به لحاظ تغییرات مورفولوژی (ریختشناسی) و مولکولی در ریههای محیطی بیمارانی که به دلیل ابتلا به این بیماری جان خود را از دست دادهاند ، نسبتا ناشناخته ماندهاست.
عفونت ناشی از کروناویروس سندرم حاد تنفسی ۲ (SARS-CoV-2) با طیف گستردهای از سندرومهای تنفسی بالینی در ارتباط است و بروز نشانههای خفیف در مسیر هوایی فوقانی تا پنومی ویروسی پیشرفته و مهلک را شامل میگردد.به لحاظ بالینی تنفس بیماران مبتلا به کرونا ویروس حاد (کووید-19) دشوار است و این گروه دچار هایپوکسمی پیشرفته(progressive hypoxemia) میشوند و سرانجام این بیماران در اغلب اوقات نیز به استفاده از دستگاه ونتیلاتور میانجامد. با استفاده از سنجش برلین(Berlin criteria) جهت سندروم دیسترس تنفسی حاد (ARDS) ،رادیوگرافینمایگراندگلاس(کدورتشیشۀمات،ground-glass opacities) ریۀمحیطی روی سیتیاسکن انجام گرفت. کدورت شیشۀ مات ، یک یافتۀ غیراختصاصی در سیتی اسکن است که به شکل یک کدورت مهآلود خود را نشان میدهد و ساختارهای زیرین خود، برونشها و عروق ریوی، را نامشخص نمیسازد.
براساس توصیف محققان در این پژوهش، بهلحاظ بافتشناسی نشانۀبارز مرحلۀ نخستین سندرم دیسترس تنفسی حاد(ARDS)، شامل تخریب گستردۀ آلوِئولار همراه با ادم(diffuse alveolar damage with edema)، خونروی(hemorrhage) و رسوب و انباشت فیبرین درون آلوئولار(intraalveolar fibrin deposition) است. تخریب گستردۀ آلوئولار یافتهای غیراختصاصی است زیرا ممکن است علل عفونی یا غیرعفونی داشته باشد که عبارتند از: کرونا ویروس سندروم تنفسی خاورمیانهای (MERS-CoV)، کرونا ویروس سندروم تنفسی حاد (SARS-Cov)، کرونا ویروس سندروم تنفسی حاد2 (SARS-CoV2) و ویروس های آنفلوآنزا.
از جمله ویژگیهای متمایز کووید-19 میتوان به تغییرات عروقی مرتبط با بیماری اشاره نمود. با توجه به تخریب گستردۀ آلوئولار، در عفونت ناشی از کرونا ویروس سندروم تنفسی حاد و کروناویروس سندروم تنفسی حاد2، تشکیل فیبرین لخته شده(fibrin thrombi) مشاهده گردید ولی، بصورت منظم و اصولی مورد مطالعه قرار نگرفته است. از نظر بالینی نیز در بسیاری از بیماران ، سطوح دی-دایمر افزایش یافت. همچنین بروز تغییراتپوستی شدید در اندام، نشاندهندۀ ترومبوتیک میکروآنژیوپاتی است. انعقاد درونرگی گسترده (Diffuse intravascular coagulation) و ترومبوز رگ بزرگ (large-vessel thrombosis) با نارسایی اندامی چند سیستمی (multisystem organ failure) در ارتباط است. تغییرات عروقی مربوط به ریههای محیطی به خوبی مشخص نشده اند اما، واسکولوپاتی در شبکه های تبادل گاز، مبتنی بر تأثیر آن روی تطبیق ونتیلاسیون و پرفیوژن، میتواند بطور بالقوه با هایپوکسمی و تأثیرات حالت بدن (بهعنوان مثال حالت درازکش-دمر) در هنگام اکسیژن رسانی در ارتباط باشد.
علیرغم تجربههای پیشین مرتبط با SARS-CoV و همچنین 2-SARS-CoV، تغییرات مورفولوژیک(ریختشناسی) و مولکولی مرتبط با این عفونتها در ریههای محیطی به خوبی مستندسازی نشدهاند. در این پژوهش به بررسی ویژگیهای مولکولی و مورفولوژیک ریهها خواهیم پرداخت. ریههای بیمارانی که در اثر ابتلا به کووید-19 جان خود را از دست داده بودند کالبدشکافی شد و با ریههای بیمارانی که در اثر ابتلا به آنفلوآنزا جان خود را از دست داده بودند و همچنین ریههای غیرعفونی مطابق سن (گروه کنترل) مقایسه شدند.
در این آزمایش هفت ریۀ بدست آمده از کالبدشکافی بیماران فوت شده در اثر کووید-19 باهفت ریۀ بدست آمده از کالبدشکافی بیماران فوت شده در اثر سندروم دیسترس تنفسی حاد(ARDS) ناشی از عفونت آنفلوآنزای(A (N1H1 و 10 ریۀ گروه کنترل (ریههای غیرعفونی مطابق با سن) را مورد ارزیابی قرار گفتند. با استفاده از آنالیز ایمونوهیستوشیمی(بافتشیمیایمنی) هفترنگ، corrosion casting، تصویربرداریمیکروسیتی(میکروتوموگرافی)،اسکنمیکروسکوپالکترونی(scanning electron microscopy) ،سنجش مستقیم و چندگانۀ بیان ژن ریه ها مورد مطالعه و بررسی قرار گرفتند. بافتشیمیایمنی نام یک فرآیند برای مکانیابی پروتئینها در یاختههای یک بافت است.
◄ نتایج :
در بیمارانی که در اثر نارسایی تنفسی ناشی از کووید-19 یا نارسایی تنفسی حاصل از آنفلوآنزا درگذشتند، الگوی مربوط به بافت شناسی ریۀ محیطی، تخریب گستردۀ آلوئولار با انفیلتراسیون سلولT پیرامونرگها( diffuse alveolar damage with perivascular T-cell infiltration ) نشان میداد.ریههای بیماران مبتلا به کووید-19 نیز ویژگیهای عروقی مشخصی را نشان دادند. این ویژگی شامل جراحت شدید اندوتلیال همراه با وجود ویروس درون سلولی(intracellular virus) و غشای سلولی ازهم گسیخته بود. ارزیابی بافتشناسی رگهای ریوی در بیماران مبتلا به کووید-19 ترومبوز وسیع با میکروآنژیوپاتی را نشان داد. در بیماران مبتلا به کووید-19 میکروترومبی مویرگی آلوئولار، 9 برابر شایعتر از بیماران مبتلا به آنفلوآنزا بود (0/001). در ریههای گروه کووید-19 میزان رگزایی( بطور عمده ازطریق مکانیسم متابولیسم آنژیوژنز) 7/2 برابر بیشتر از رگزایی در گروه آنفلوآنزا بود(P<0.001).
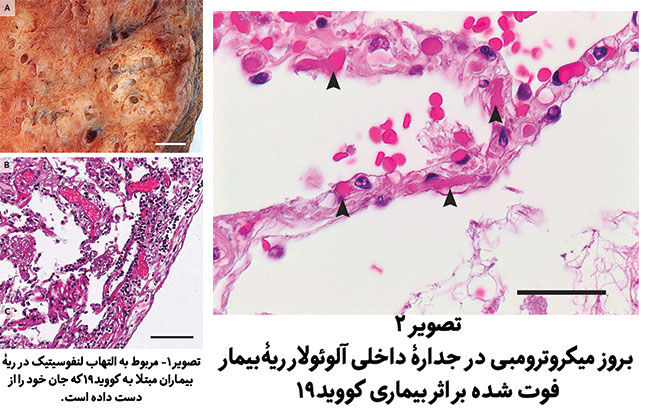
در تمام نمونههای ریههای گروه کووید-19 این نشانهها مشاهده شد: تخریب گستردۀ آلوِئولار همراه با نکروز سلولهای پوششی آن، هیپرپلازی(hyperplasia)، پنوموسیت نوع 2 و انباشت فیبرین درونرگی خطی (شکل 1). تغییرات در 4 مورد از 7 مورد کانونی بود و فقط ادم خفیف بینابینی(mild interstitial edema) مشاهده گردید. در سه نمونۀ باقیمانده، انباشت(رسوبات) همگن فیبرین(homogeneous fibrin) و اِدم علامتدار بینابین همراه با تشکیلات درون آلوئولار زودرس(marked interstitial edema with early intraalveolar organization) مشاهده گردید.
در نمونههای گروه آنفلوآنزا تخریب گستردۀ آلوئولار (قرمز رنگ) با ادم بینابینی وسیع و رسوب گستردۀ فیبرین در تمام نمونهها مشاهده شد. علاوه بر این در گروه آنفلوآنزا سه مورد از نمونهها دارای آرایش کانونی و التهاب جذبی (resorptive) بودند. این تغییرات در ریههایی که وزن بالاتری داشتند، در گروه آنفلوآنزا بازتاب بیشتری داشت.
◄ ترومبوز و میکروآنژیوپاتی:
سیستم عروق ریوی ریه های گروه کووید-19 و گروه آنفلوآنزا بااستفاده از روشهایی با نام رنگآمیزی هماتوکسیلین - آئوزین، تریکروم و رنگآمیزی ایمونوهیستوشیمی(immunohistochemical staining) تحت ارزیابی قرارگرفتند. آنالیز عروق پیش مویرگی نشان داد که 4 ریه از 7 ریۀ گروه کووید-19 و 4 ریه از 7 ریۀ گروه آنفلوآنزا، ترومبی بصورتی پایدار در سرخرگ ریوی با شعاع 1 تا 2 میلیمتر وجود دارد و هیچ انسداد لومینال(luminal obstruction) مشاهده نشد. ترومبیِ فیبرین مویرگهای آلوئولار را میتوان در ریههای تمام افراد دو گروه مشاهده نمود (شکل 2). میکروترومبی مویرگی آلوئولار(Alveolar capillary microthrombi) در بیماران گروه کووید-19 ، 9 برابر گروه آنفلوآنزا شایعتر بود. ترومبی درون عروقی در ونولهای پس مویرگی(Intravascular thrombi in postcapillary venules ) (با قطر کمتر از 1 میلیمتر) گروه کووید-19 کمتر از بیماران گروه آنفلوآنزا بود (16±35 vs. 14±12, P=0.02). در مقایسه با چهار ریه از گروه آنفلوآنزا ، دو ریه از گروه کووید-19 تمام بخشهای سیستم عروقی درگیر بودند. در سه ریۀ گروه کووید-19 و سه ریۀ گروه آنفلوآنزا ترکیبی از ترومبی سیاهرگی و مویرگی بدون ترومبی سرخرگی مشاهده گردید.
یافته های بافتشناسی بااستفاده از میکروسیتیاسکن سه بعدی نمونههای ریوی نشان داد که رگهای پیش مویرگی و پس مویرگی ریه های بیماران گروه کووید-19 و گروه آنفلوآنزا تقریبابطور کامل مسدود شدهاند.
◄ آنژیوژنز:
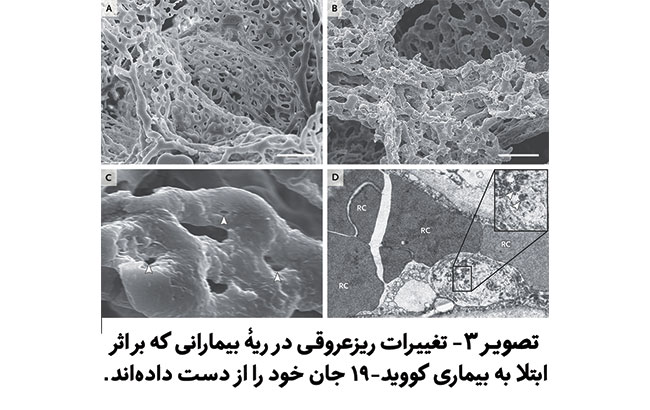
ساختار ریزعروقی (Microvascular) ریههای بیماران کووید-19 ، بیماران آنفلوآنزایی و گروه کنترل سالم ، توسط میکروسکوپ الکترونی و microvascular corrosion casting مورد ارزیابی قرارگرفت. در روش microvascular corrosion casting با استفاده از ساختار سهبعدی، رگهای خونی را در اندام انسان و حیوان شبیه سازی مینمایند. در ریههای گروه کووید-19 ، دارای سیستم عروقی از حالت طبیعی خارج شده و با تغییرشکل (Deform) ساختاری مویرگهاهمراه بود (شکل 3). مویرگهای کشیدهشده (Elongated capillaries) در ریههای گروه کووید-19 نشانگر تغییر ناگهانی در گنجایش و حضور ستونهای intussusceptive در داخل مویرگها بود (شکل 3c). با استفاده از میکروسکوپ الکترونی (Transmission electron microscopy)، اندوتلیوم گروه کووید-19 نشاندهندۀ تخریب فراساختاری اندوتلیوم و همچنین حضور کروناویروسِ سندروم تنفسی حاد2 درونسلولی بود (شکل 3D). همچنین ویروس میتواند در فضای خارج سلولی نیز شناسایی شود.
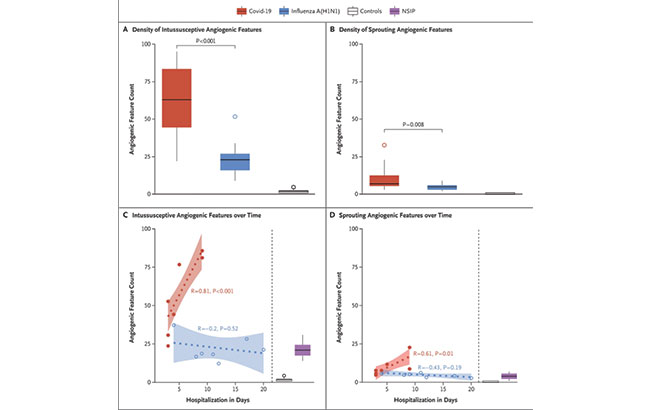
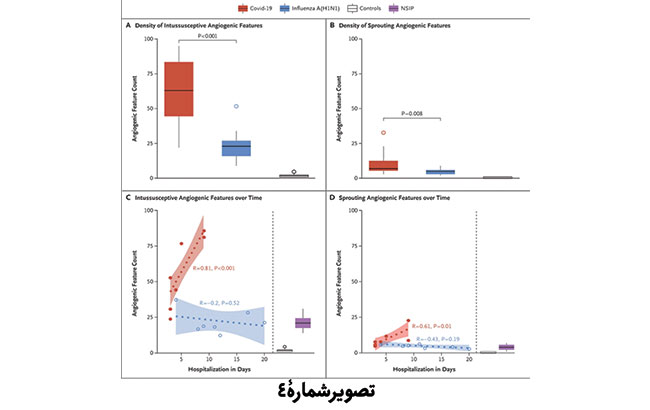
در ریههای گروه کووید-19 چگالی درهمرفتگی ویژگیهای آنژیوژنیک (رگزایی) بطور قابل توجهی بزرگتر از چگالی ریههای گروه آنفلوآنزا ، یا گروه کنترل بود (P<0.001 برای هر دو گروه مقایسه شد) (شکل 4A). چگالی رگزایی ازطریق جوانهزنی(density of features of conventional sprouting angiogenesis) در گروه کووید-19 بیشتر از گروه آنفلوآنزا بود (شکل 4B). با ترسیم ویژگی آنژیوژنیک (رگزایی) ریوی بهعنوان تابع طول مدت بستری در بیمارستان مشخص شد که با افزایش دورۀ بستریشدن در بیمارستان میزان درهمروی رگزایی افزایش مییابد (P<0.001) (شکل 4c). در مقابل در ریههای گروه آنفلوآنزا درهمروی رگزایی کمتر بود و با گذشت زمان افزایش نیافت (شکل 4C). برای رگزایی ازطریق جوان هزنی الگویی مشابه مشاهده گردید (شکل 4D).
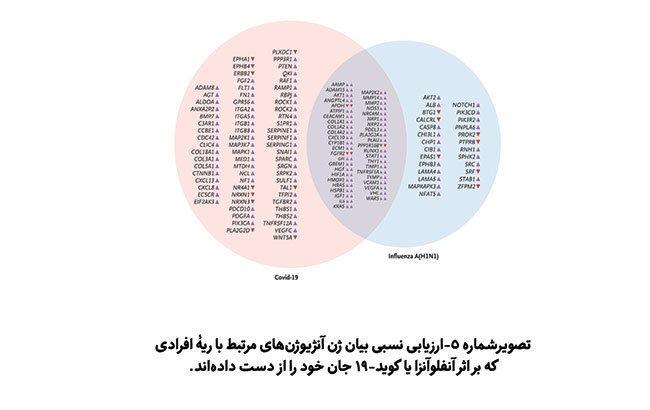
در یک ارزیابی چندگانۀ بیان ژن مربوط به رگزایی بهوسیلۀ فنآوری cCounter Pan Cancer Progression (فنآوریهای نانواسترینگ) 323 مورد ژن بررسی شدند. این بررسی نشانگر وجود تفاوت میان نمونههای بدستآمده از گروه کووید-19 و گروه آنفلوآنزا بود. تنها در گروه کووید-19 مجموع 69 ژن و در گروه آنفلوآنزا 26 ژن مربوط به رگزایی بصورت افتراقی تنظیم شدند. 45 ژن دارای تغییرات مشترک در بیان ژن بودند (شکل 5).
◄ نتیجه گیری:
در این نمونۀ کوچک تحت بررسی، رگزایی عروقی(vascular angiogenesis) پاتوبیولوژی ریوی در کووید-19 متمایز از رگزایی عروقی در عفونت ویروسی آنفلوآنزا (با همان شدت کووید-19) است. در هر روی جامعیت و پیچیدگیهای بالینی مشاهدات و تجربیات پیرامون کووید-19 نیازمند انجام تحقیقات بیشتری است و به طور حتم درآینده به نتایج قابل توجهی خواهیم رسید.
Ref:The New England Journal Of Medicine

ثبت نظر